热分析是科研表征中常见的手段。所谓热分析,指通过控制样品温度的改变,来分析其相应物理化学性质的改变。最为常见的热分析手段有三种热重分析(TG)、差热分析(DTA)和差示扫描量热法(DSC)。具体分析和讲解如下:
1. 如何正确选择热分析方法?
三种热分析方法各有所长,可以单独使用、也可以联合使用。具体如何选择,我们首先从定义出发,了解这些表征手段。
TG:在程序控温下,测量样品的质量(m)随温度的变化。如果你需要知道,样品在升温或者降温过程中,样品质量的变化(比如吸附、脱附、分解等),请选择TG。比如工业催化剂中常会有积碳现象,通过TG表征可以确定积碳量。
DTA:在程序控制温度下,测量参比物和样品温差(△T)随温度(T)的变化。DTA与TG的区别在于测量值从质量变为温差。之所选择测试温差,是因为升温过程中发生的很多物理化学变化(比如融化、相变、结晶等)并不产生质量的变化,而是表现为热量的释放或吸收,从而导致样品与参比物之间产生温差。DTA能够发现样品的熔点、晶型转变温度、玻璃化温度等等信息。
DSC: 在程序控制温度下,测量给于参比物和给予样品的能量之差(△Q)随温度(T)的变化。在整个测试过程中,样品和参比物温差控制在极小的范围内。当样品发生物理或者化学变化时,控温装置将输入一定功率能量,以保持温度平衡。可以简单的将DSC看成是DTA的升级版。DSC也确实是从DTA发展而来。传统的DTA仪器因为样品池材质的关系,只能测温差,无法准备测量热和焓的变化。后期通过改变材质和结构,使得从温差转变为能量差成为可能(热流型)。最后又出现一种直接测量输入热量差的DSC(功率补偿型)。DSC的优点在于灵敏度高、可以定量测量焓、比热容等物理量。
2. 数据如何分析?
TG:典型的TG图如下图1所示:
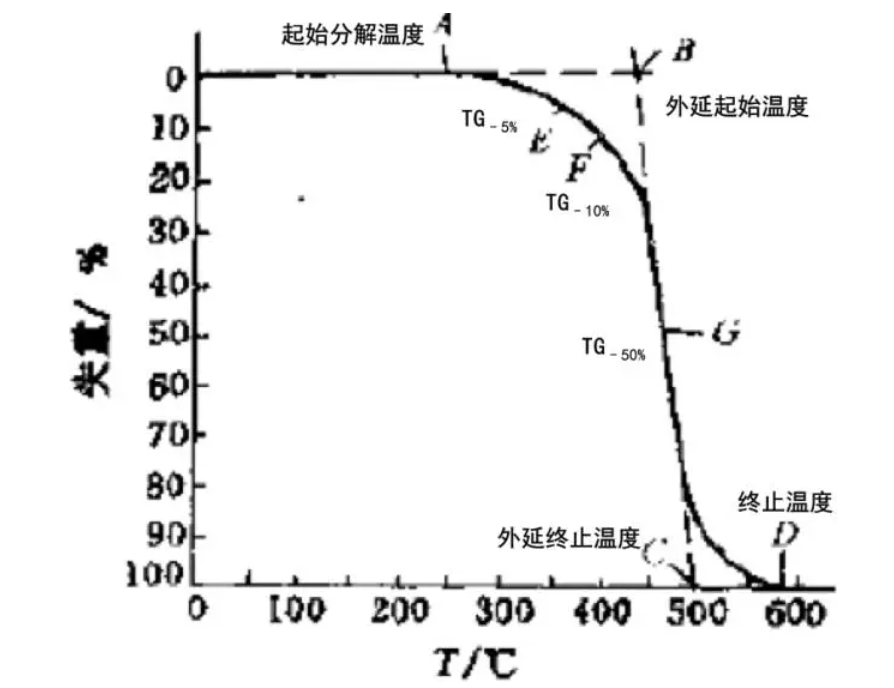
图1
其中最重要的信息是失重的温度点和失重的比例。根据你所测试材料的性质和这些温度点、失重比例,可以推测所发生的物理化学变化。比如100 – 150 摄氏度之间常对应物理吸附的水。200 – 350摄氏度范围的失重常对应有机物的分解。
DTA:曲线图如下图2所示:
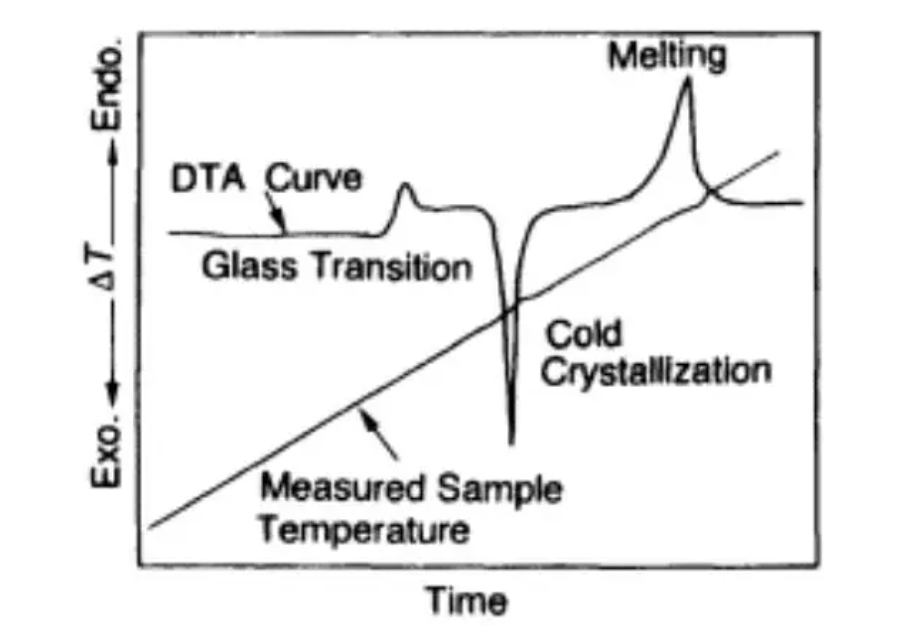
图2
图中的纵坐标为温差,横坐标为温度或者时间。对于DTA曲线的分析主要有三部分:峰位、峰的形状和峰的个数。峰位用于判断发生变化的温度(比如相变温度、玻璃化温度、分解温度等)、峰的形状用于判断吸热还是放热,一般规定向上为放热、向下为吸热。每个峰都对应一种化学或物理变化。
DSC: 如图3.
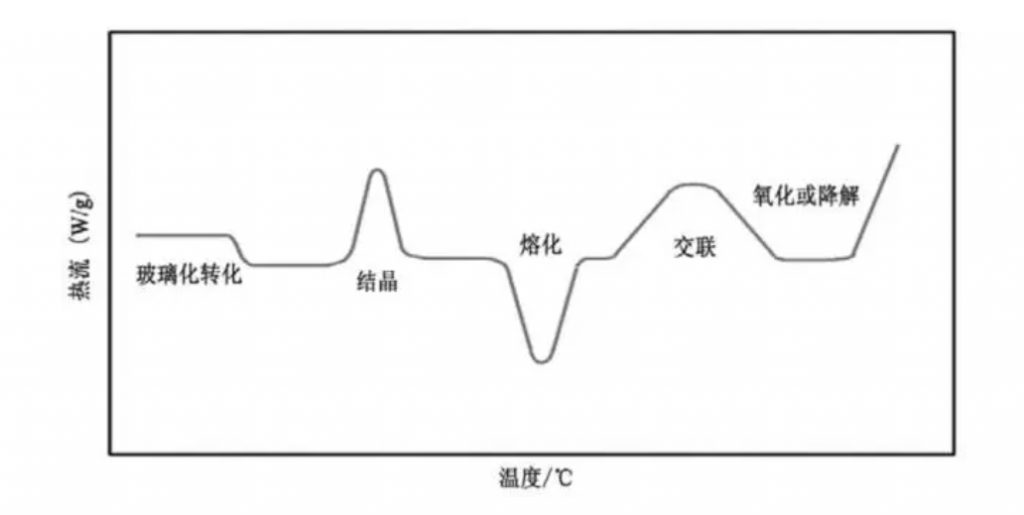
图3
从形状来看,DSC曲线和DTA很相似,但纵坐标不同。DSC图中纵坐标热流量(单位为mW或者mJ/S)。从积分峰面积就能算出焓变。如果参比物比热容已知还可以算出样品的比热容。在实际应用中TG常和DTA或者DSC连用。
3. 测试中的注意事项
在进行热分析测试时,需要注意三个方面:1.升温速率,升温速率不易过快。否则会导致基线不稳,温度测试不准确等问题。一般选择在10 – 20 摄氏度/min。2.气氛的选择:这需要根据要求选择。比如需要排除O2的干扰,则可以选择N2气氛。还可以选择还原性气氛。3. 加盖与否:a. 对于物理效应(熔融、结晶、相变等)的测试或偏重于DSC的测试,通常选择加盖。对于未知样品,出于安全性考虑,通常选择加盖。b. 对于气固反应(如氧化诱导期测试或吸附反应),使用敞口坩埚(不加盖)。c. 对于有气体产物生成的反应(包括多数分解反应 )或偏重于TG的测试,在不污染损害样品支架的前提下,根据反应情况与实际的反应器模拟,进行加盖与否的选择。对于液相反应或在挥发性溶剂中进行的反应,若反应物或溶剂在反应温度下易于挥发,则应使用压制的Al坩埚(温度与压力较低)或中压、高压坩埚(温度与压力较 高)。对于需要维持产物气体分压的封闭反应系统中的反应同样如此。
4. 实例分析:
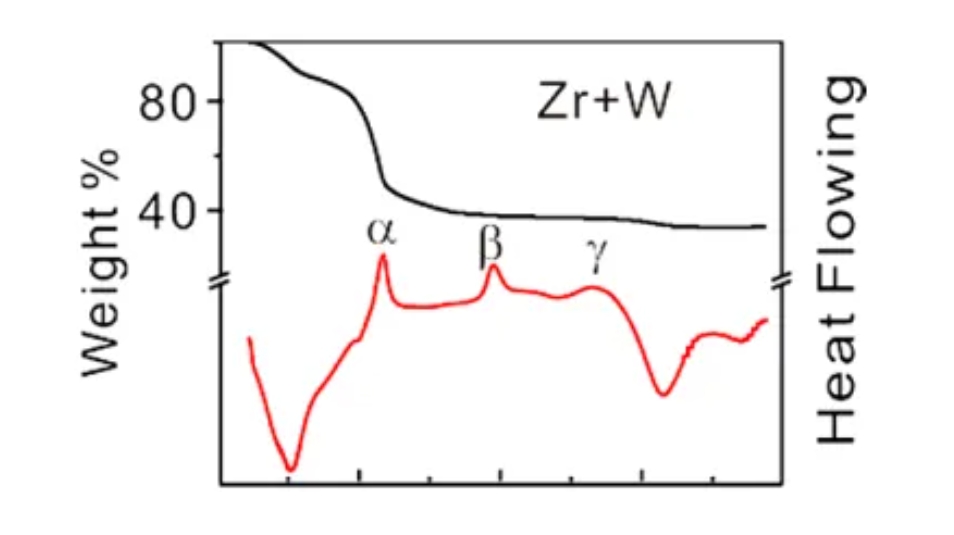
图 4
图4为WZrOx复合催化剂的TG和DSC图。150度之前的质量损失(TG图)为催化剂表面吸附水的脱除。310 – 340 C为有机大分子的分解,对应DSC图中的α放热峰。350度之后,TG线中没有任何质量损失。DSC曲线上的β放热峰对应ZrO2的结晶峰。结合其他表征,作者将γ峰归结为催化剂中形成很细小的W-ZrO2 Cluster。
来源:研之成理微信公众号

永清石墨烯研究院检测中心简介
检测中心围绕石墨烯和新能源材料相关实验和检测分析搭建实验室业务能力,涵盖材料微观形貌、热学性能、理化性能、力学性能和电池电性能等检测项目,满足企业大部分研发、中试检测需求。检测认证中心通过CNAS认可实验室认证,实验室面积达1600m2,配备日立冷场发射扫描电子显微镜、耐驰激光导热分析仪、梅特勒同步热分析仪等180多台套仪器设备。检测中心秉持“公正、诚信、科学、高效”的原则,竭诚为国内外企业和高校科研院所提供高质量的检测服务。
